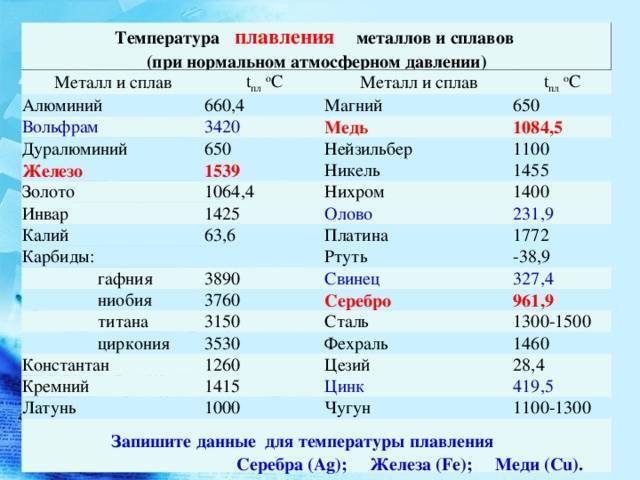
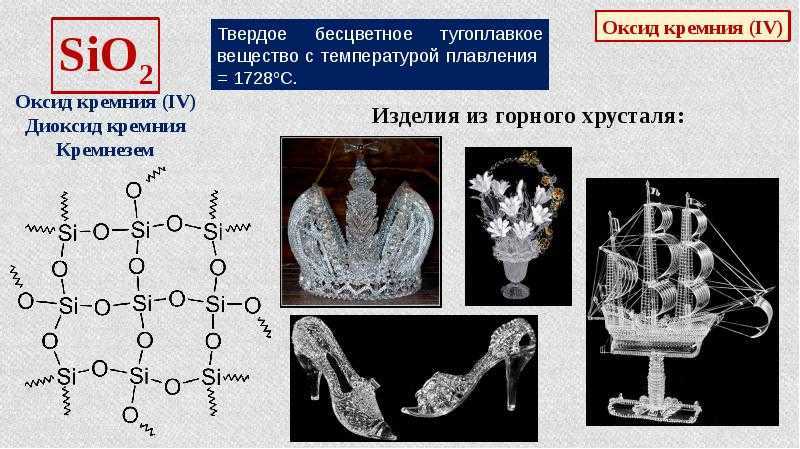
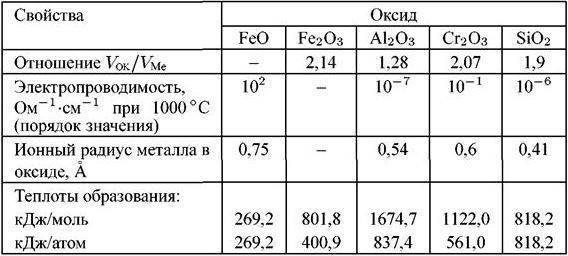
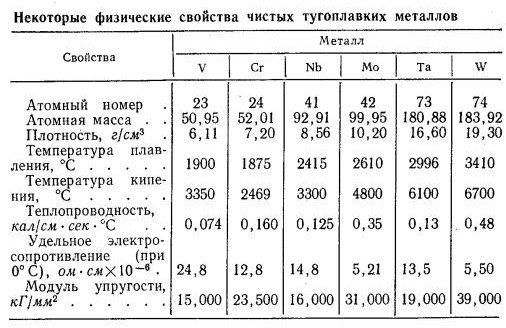
Стадии обработки прутков
Если длина штабика не превышает 10−15 см, обработке подвергаются детали диаметром 7 мм. Для получения такого размера поднимают температуру до 1500 градусов. Дополнительным нагревателем выступает молибден.
Для получения изделия диаметром 4,5 мм рабочая температура уменьшается до 1300 °C. Сечение 2,75 мм получается при аналогичной температуре.
Все вольфрамовые прутки подразделяются на несколько групп. Они обозначаются:
- ВТ.
- ВЛ.
- ВИ.
- ВА.
- ВЧ.
Для изготовления прутков ВТ, ВЛ, ВИ используется очень высокая температура. Она намного ниже при получении вольфрамовых изделий ВЧ и ВА.
Основой этого материала стали вольфрамовые слитки, изготовленные методом плавления. Горячая обработка таких слитков не делается. Это связано с их структурой, в которую входят грубые кристаллы. При горячей обработке металл начинает трескаться.
Как подготовить покрытие заготовки карбида вольфрама?
Во многих случаях готовая деталь должна быть покрыта. Покрытие обеспечивает смазывающую способность и повышенную твердость и обеспечивает диффузионный барьер для подложки, который предотвращает окисление при воздействии высоких температур. Матрица карбида вольфрама имеет решающее значение для характеристик покрытия. В дополнение к основным характеристикам порошка настраиваемой матрицы поверхностные свойства подложки могут быть подобраны путем химического отбора и модификации процесса спекания. Благодаря движению кобальта более кобальт может быть обогащен самым наружным слоем поверхности лопасти толщиной 20-30 мкм относительно остальной части заготовки, тем самым придавая более хорошую ударную вязкость поверхностному слою подложки, имеет сильное сопротивление деформации.
Производители инструмента, основанные на собственных производственных процессах (такие как методы депарафинизации, скорости нагрева, время спекания, температуры и науглероживающие напряжения), могут предъявлять особые требования к классам используемого порошка карбида. Некоторые изготовители инструмента могут спекать заготовки в вакуумных печах, в то время как другие могут использовать спекающие печи с горячим изостатическим прессованием (HIP) (которые герметизируют заготовку в конце технологического цикла для устранения остатков). Pore). Заготовка, спеченная в вакуумной печи, также может быть подвергнута процессу горячего изостатического прессования для увеличения плотности заготовки. Некоторые производители инструмента могут использовать более высокие температуры спекания в вакууме для увеличения спеченной плотности смесей с более низким содержанием кобальта, но этот подход может сделать грубую микроструктуру.
Для поддержания мелкого размера зерна можно использовать порошок с меньшим размером частиц карбида вольфрама. Чтобы соответствовать конкретному производственному оборудованию, условия депарафинизации и науглероживающее напряжение также имеют разные требования к содержанию углерода в порошке карбида вольфрама.Все эти факторы оказывают решающее влияние на микроструктуру и свойства материала инструмента из карбида вольфрама, который спекается. Поэтому существует необходимость в тесной связи между производителем инструмента и поставщиком порошка, чтобы обеспечить его изготовление в соответствии с инструментом. Индивидуальный производственный процесс изготовленный на заказ порошок карбида вольфрама. Поэтому неудивительно, что существуют сотни различных марок карбидов. Например, ATI Alldyne производит более 600 различных марок порошков, каждый из которых специально разработан для предполагаемого пользователя и конкретного использования.
Карбид вольфрама по сравнению с вольфрамом.
Люди часто используют термины вольфрам и карбид вольфрама взаимозаменяемо. Однако есть различия в свойствах этих двух материалов.
Во-первых, вольфрам легче царапается.
Кольца, изготовленные только из него, не очень устойчивы к царапинам, так что вы не должны ожидать, что они со временем останутся такими же блестящими.
Во-вторых, вольфрамовые ювелирные изделия часто содержит кобальт, в то время как карбид вольфрама, как правило, смешан с никелем. Проблема заключается в том, что, когда кобальт вступает в контакт с кожей, металл может вызвать раздражение.
Кроме того, кобальт может окислиться и заставить ваши драгоценности изменить цвет.
Как используется
Свойства вольфрама обозначили главного потребителя. Это металлургия. Она создает конечный продукт и исходники для других отраслей промышленности.
Порошковый вольфрам – основа либо компонент твердых, жаропрочных износоустойчивых сплавов, премиальных марок сталей.
Металл, сплавы
Из тугоплавкого металла и сплавов создают широкий ассортимент продукции:
- Узлы и детали авиационных, ракетных двигателей.
- Элементы электровакуумных приборов (кинескопы, нити накаливания).
Нить накаливания из вольфрама
- Нагреватели вакуумных печей.
- Электроды для аргонно-дуговой сварки. Они не плавятся, создают прочный сварной шов. Пригодны для материалов любого состава (цветные металлы, легированные стали, другие).
- Емкости для радиоактивных продуктов. Здесь решающими оказались преимущества металла перед свинцом.
- Хирургический инструментарий.
Характеристики металла подошли оборонному комплексу: танковая, торпедная броня, крупнокалиберные снаряды, пули. А также суперскоростные роторы гироскопов, контролирующих траекторию полета баллистических ракет.

Вольфрам в слитках
Соединения
Обширен спектр применения вольфрамовых соединений:
- Без дителлурида невозможно преобразование тепла в электричество.
- Карбид – основа сплавов и композитов для механической обработки металлов и неметаллов. У горнодобытчиков, нефтяников, газовиков – для бурения скважин.
- Сульфид – термостойкая (до 500°C) смазка.
- Трехокись – материал для создания электролита топливных элементов, работающих при повышенных температурах.
Соединения вольфрама закупают производители лаков, красок, текстиля.
Другие формы
Изотоп W184 – компонент сплавов с изотопами урана. Из них делают ракетные двигатели на ядерном топливе.
Радионуклид искусственного происхождения (W185) востребован как детектор излучений (включая рентгеновское) ядерным сегментом физики и медицины.
История открытия и изучения
Свое название металл получил от минерала вольфрамит. Его начали добывать в XVI веке. Тогда его называли «волчьей пеной». Вольфрам часто встречался в оловянных рудах, мешал выплавлять этот металл. Он переводил его в пену шлаков.
Первое научное упоминание о нахождении нового химического элемента появилось в 1781 году. Тогда знаменитый химик из Швеции Карл Шееле работал с минералом шеелит. Он обрабатывал его азотной кислотой, в ходе чего получил новый химический элемент с желтым оттенком. Он назвал его «тяжелым камнем». Через два года, братья Элюар получили из саксонского минерала новый металл.
 Вольфрамит
Вольфрамит
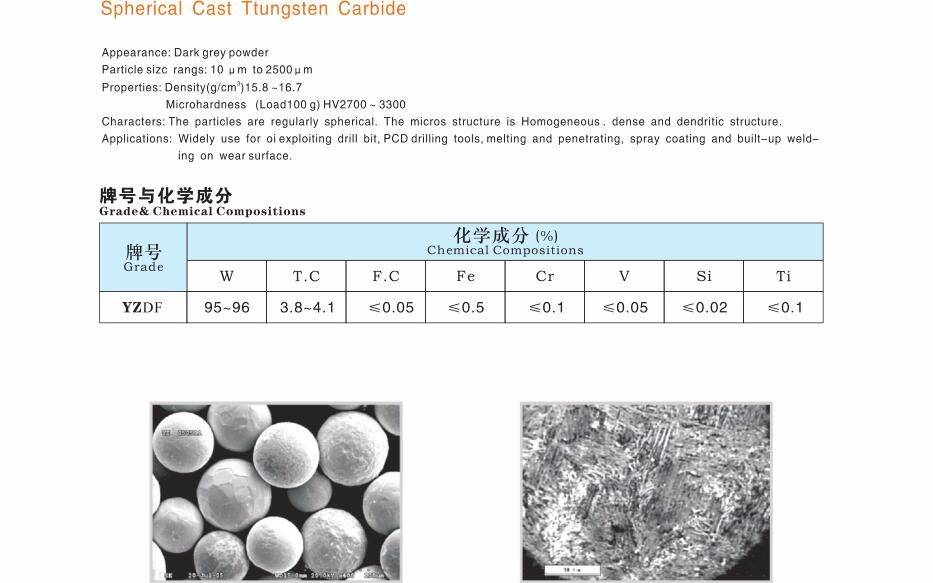
Свойства
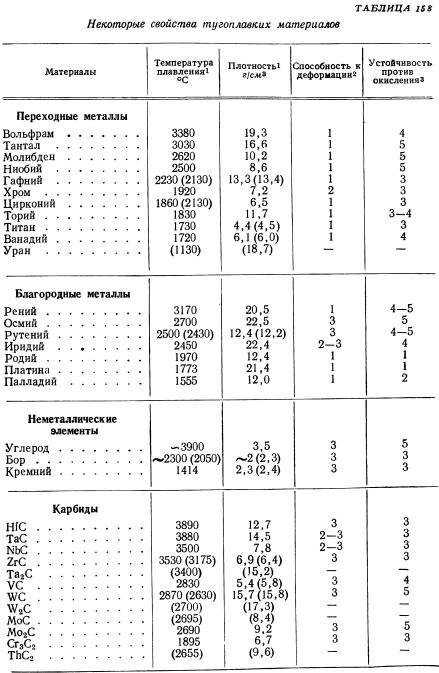
Рассматриваемое вещество представлено серым порошком в двух кристаллографических вариантах: с кубической (полукарбид) и гексагональной (монокарбид) решетками. Обе модификации встречаются в температурном диапазоне 2525 — 2755°С. Вторая фаза ввиду отсутствия области гомогенности при отклонении от стехиометрического состава образует графит или переходит в W2C, а при температуре более 2755°С разлагается до углерода и первой фазы. Последняя отличается обширной областью гомогенности, сокращающейся при снижении температуры.
Монокарбид вольфрама менее тверд в сравнении с полукарбидом, но способен формировать кристаллы. Второй вариант значительно более температуро- и износоустойчив. К тому же он способен к внедрению в твердые растворы.
Карбид вольфрама отличается хрупкостью, но под влиянием нагрузки проявляет пластичность полосами скольжения.
Кристаллы рассматриваемого вещества характеризуются анизотропией твердости от 13 до 22 ГПа на разных кристаллографических плоскостях.
Монокарбид имеет температуру плавления 2870°C, кипения — 6000°C. Его молярная теплоемкость равна 35,74 Дж/(моль-*К), теплопроводность — 29,33 кДж/моль. Плотность карбида вольфрама данного типа составляет 15,77 г/см3.
Несмотря на то, что температура плавления большая, термостойкость рассматриваемого материала низка. Это обусловлено отсутствием термического расширения ввиду жесткой структуры. При этом карбид вольфрама характеризуется высокой теплопроводностью. С повышением температуры данный параметр у монокарбида возрастает вдвое быстрее, чем у полукарбида.
Кольцо из карбида вольфрама
Рассматриваемые материалы имеют хорошую электропроводность, особенно полукарбид (в 4 раза выше, чем монокарбид). Удельное электросопротивление возрастает с повышением температуры, но при этом снижается упругость. Это обуславливает обрабатываемость электрофизическими методами. Так, при введении источника тепла в области обработки возрастает температура, способствуя размеренному разрушению структуры материала.
Твердость определяется температурой формирования карбидов в вольфрамовом порошке и (в меньшей степени) их пористостью. С ростом температуры увеличивается подвижность атомов составляющих соединения элементов, вследствие чего устраняются дефекты в зернах. Анизотропия параметров карбидов вольфрама меньше, чем для металлов. К тому же данные материалы отличаются наилучшей для тугоплавких металлов упругостью, которая увеличивается с ростом пористости. Однако пластичность низкая (до 0,015%).
Микроструктура карбида вольфрама
Карбид вольфрама характеризуется стойкостью к многим кислотам, а также их смесям при обычной температуре, но растворим в некоторых кислотах при кипении. Не подвержен растворению в 20% и 10% гидроксиде натрия. Ввиду высокой летучести оксида вольфрама начинает окисляться при 500 — 700°C и завершает окисление при более 800°C.
Наконец, ввиду химической инертности данное соединение нетоксично.
Применение вольфрама в промышленности
Вольфрам начали активно применять в различных сферах промышленности не так уж и давно. На протяжении долгого времени он не мог найти практического применения, но сейчас больше половины всего вольфрама идет на производство вольфрамовых сплавов различной прочности. Перечислим сферы и области применения вольфрама более подробно:
— электротехническая промышленность. Вольфрам незаменим в данной сфере, так как из его изготавливают нити накалывания электрических ламп, катоды рентгеновских трубок и различные детали для радиоламп.
— химическая промышленность. В данной сфере вольфрам применяют в качестве сырья для изготовления пигментов, красок и смазочных материалов. Помимо этого, данный неметаллический элемент применяют как катализатор.
— военная промышленность. Вольфрам был одним из основных сырьевых материалов в данной сфере во времена Первой Мировой войны. Его применяют для производства пуль, орудийной стали и бронебойных снарядов.
— автомобильная промышленность. Вольфрам выступает в качестве легированного элемента некоторых видов стали. Он придает стали уникальных свойств и позволяет использовать её для производства автомобильных прочных рессор. Более подробно об этом можно узнать в нашей статье «Сферы и области применения стали».
— железнодорожная промышленность. Вольфрамовая сталь применяется для производства железнодорожных рельс и вагонов. Такие рельсы могут выдержать очень большие нагрузки. Кроме того, их срок эксплуатации намного больше, чем из других видов стали.
— металлургическая промышленность
Наиболее важное предназначение вольфрама в металлургии – это легирование им сталей, а также производство твердых сплавов
Основные характеристики
Как самый тугоплавкий металл, вольфрам имеет специфические свойства:
- Температура плавления вольфрама — примерно соответствует температуре солнечной короны — 3422 °С.
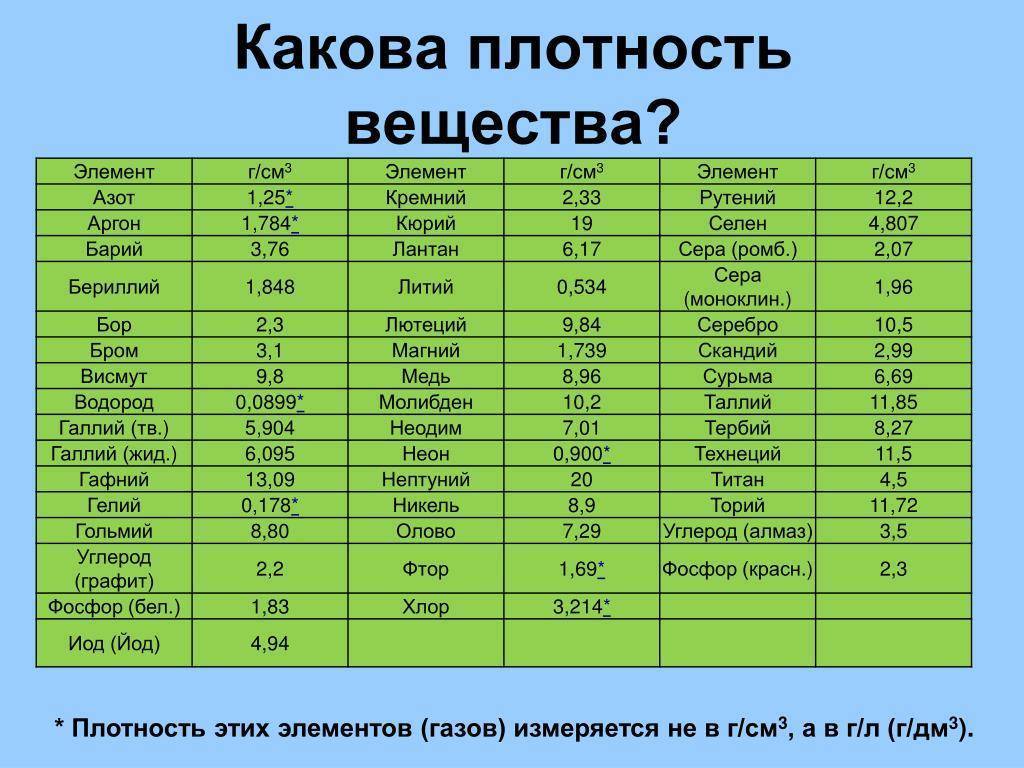
- Вместе с этим, плотность чистого вольфрама ставит его в один ряд с наиболее плотными металлами. Его плотность практически равна плотности золота — 19,25 г/см3.
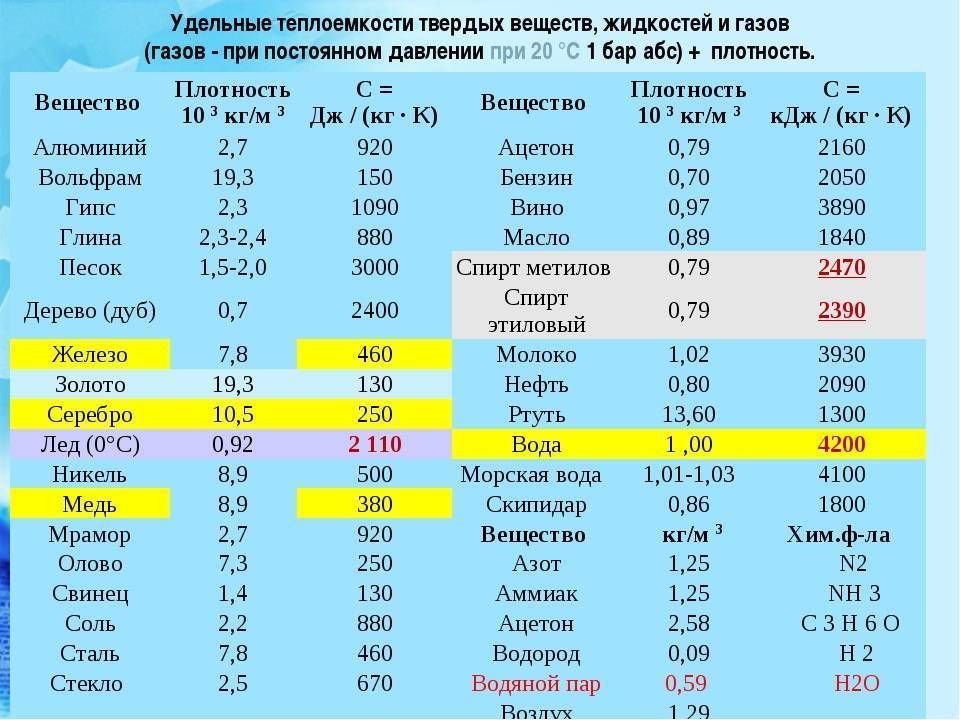
- Теплопроводность вольфрама зависит от температуры и составляет от 0,31 кал/см·сек·°С при 20°С до 0,26 кал/см·сек·°С при 1300°С.
- Теплоемкость также близка к золоту и составляет 0.15·103 Дж/(кг·К).
Металл имеет кубическую объемноцентрированную кристаллическую решетку. Несмотря на высокую твердость, вольфрам в нагретом состоянии очень пластичен и ковок, что позволяет изготавливать из него тонкую проволоку, имеющую широкое применение.

Вольфрамовая проволока
Имеет серебристо-серый цвет, который не меняется на открытом воздухе, поскольку вольфраму присуща высокая химическая стойкость, а с кислородом он реагирует только при температуре выше красного каления.
Химические свойства элемента, как правило, начинают проявляться при нагреве выше нескольких сотен градусов. В обычных условиях он не взаимодействует с большинством известных кислот, кроме смеси плавиковой и азотной кислот. В присутствии определенных окислителей может реагировать с расплавами щелочей. При этом для начала реакции требуется нагрев до температуры 400 — 500 °С, а далее реакция идет бурно, с выделением тепла.
Некоторые соединения, особенно карбид вольфрама, обладают очень высокой твердостью и находят применение в металлургическом производстве для обработки твердых сплавов.
Приведенные характеристики вольфрама определяют специфику областей применения металла, как в чистом виде, так и в составе различных сплавов и химических соединений. Вольфрам входит в состав многих жаростойких сплавов в качестве легирующей добавки для повышения твердости, температуры плавления и коррозионной стойкости. Близость плотности и теплоемкости вольфрама и золота теоретически может служить для подделки золотых слитков, однако это легко можно выявить при измерении электрического сопротивления и при переплавке золотого слитка.
Получение вольфрама
В чистом, самородном виде металл в природе не встречается. Большинство месторождений образовано оксидами. Содержание соединений в пересчете на чистый металл в рудном месторождении составляет 0.2 — 2%. Химическая стойкость и высокая температура плавления допускают получение вольфрама из руды только при использовании специфических методик.

Вольфрамовые прутки
В основе большинства методов промышленного получения вольфрама лежит восстановление металла из его оксида. Первая стадия производства состоит в обогащении вольфрамосодержащей руды. Затем при помощи операций выщелачивания и восстановления получают оксид WO3, который восстанавливают до чистого металла в атмосфере водорода. Температура процесса составляет около 700 °С.
В результате реакции получается тонкодисперсный металлический порошок. Высокая температура плавления не позволяет оформить металл в виде слитков, поэтому порошок вольфрама сначала прессуют под высоким давлением, а затем спекают в среде водорода, используя нагрев до температуры 1300 °С. Через полученные бруски пропускают мощный электрический ток. В результате высокого переходного сопротивления между зернами металла происходит нагрев и плавление заготовки.
Очистку полученного слитка производят методом зонной плавки, подобно технологии получения сверхчистых полупроводников. Производство вольфрама по данной технология позволяет получить металл высокой степени чистоты без дополнительных операций очистки.
При производстве сплавов, все составляющие добавляются еще перед стадией прессования порошка, поскольку в дальнейшем это сделать уже невозможно. В процессе прессовки, спекания и дальнейшей обработки заготовки (прессование, прокатка) обеспечивается равномерное распределение примесей в сплаве.

Вольфрам
Обработка вольфрама производится при температурах около полутора тысяч градусов. При таком нагреве металл становится очень пластичным и допускает ковку, штамповку. Тонкая проволока для спиралей ламп накаливания изготавливается методом волочения. При этом кристаллы металлы располагаются вдоль проволоки, повышая ее прочность. Поскольку к спиралям ламп предъявляются высоки требования по однородности, вольфрамовый провод дополнительно подвергают операциям электрохимического полирования.
(3) КАРБИДНЫЙ СПЛАВ ТИПА
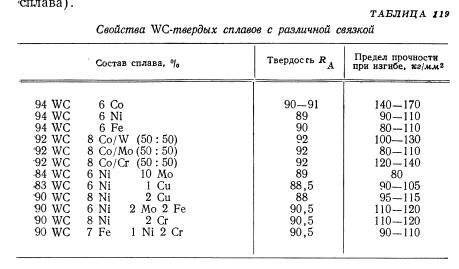
Эти марки в основном используются для резки стальных деталей, которые обычно имеют содержание кобальта в 5-10% и диапазон размеров зерен 0,8-2 мкм. Добавляя от 4% до 25% карбида титана (TiC), склонность карбида вольфрама (WC) диффундировать к поверхности стального лома может быть уменьшена. Прочность инструмента, износостойкость кратера и сопротивление термическому удару можно улучшить, добавив не более 25% карбида тантала (TaC) и карбида ниобия (NbC). Добавление таких кубических карбидов также увеличивает покраснение инструмента, что помогает избежать термической деформации инструмента во время сверхпрочной резки или другой обработки, когда режущая кромка может создавать высокие температуры. Кроме того, карбид титана может обеспечить места зародышеобразования во время спекания, улучшая однородность распределения кубического карбида в заготовке.
В целом, сплавы типа карбида имеют диапазон твердости HRA91-94 и прочность на разрыв в поперечном направлении 150-300 тыс.фунтов / кв.дюйм. По сравнению с простым типом износостойкость сплава имеет низкую износостойкость и низкую прочность, но его износостойкость лучше. Сплавы сплавов могут быть разделены на C5-C8 в системе класса С и могут классифицироваться в соответствии со стандартами класса P и M в системе качества ISO. Сплавы сплавов с промежуточными свойствами можно классифицировать как общие классы (например, C6 или P30) для токарной обработки, нарезания резьбы, строгания и фрезерования. Самые твердые сорта могут быть классифицированы как мелкие сорта (например, C8 и P01) для отделки и расточки. Эти сорта обычно имеют меньший размер зерна и более низкое содержание кобальта для достижения желаемой твердости и износостойкости. Однако аналогичные свойства материала могут быть получены путем добавления большего количества кубических карбидов. Наиболее устойчивые марки могут быть классифицированы как грубые (например, C5 или P50). Эти сорта обычно имеют средний размер частиц и высокое содержание кобальта, а количество добавленного кубического карбида также мало для достижения желаемой вязкости за счет ингибирования распространения трещины. В прерванном процессе поворота эффективность резания может быть дополнительно улучшена за счет использования богатого кобальтом сорта, имеющего более высокое содержание кобальта на поверхности резака.
Сплавы сплавов с низким содержанием карбида титана используются для обработки нержавеющей стали и ковкого чугуна, но могут также использоваться для обработки цветных металлов (таких как суперсплавы на основе никеля). Эти сорта обычно имеют размер зерна менее 1 мкм и содержание кобальта от 8% до 12%. Сорта с более высокой твердостью (например, M10) могут использоваться для обработки ковкого чугуна; марки с лучшей ударной вязкостью (например, M40) могут использоваться для фрезерования и строгания стали или для обработки нержавеющей стали или суперсплавов.
Сплавы карбида сплава также могут использоваться для неметаллической резки, прежде всего для изготовления износостойких деталей. Эти сорта обычно имеют размер частиц 1,2-2 мкм и содержание кобальта 7% -10%. При производстве этих сортов обычно добавляется большая доля переработанных материалов, что приводит к повышению экономической эффективности при применении изношенных деталей. Изношенные детали требуют хорошей коррозионной стойкости и высокой твердости. Эти марки могут быть получены путем добавления никеля и карбида хрома при производстве таких сортов.
Соединения вольфрама с галогенами.
Вольфрам образует различные соединения с галогенами. Наибольшее значение из них имеют его хлориды. Порошкообразный металлический вольфрам непосредственно соединяется с хлором при нагревании до температур порядка 500 °C.Шестихлористый вольфрам представляет собой синевато-черные с фиолетовым оттенком кристаллы, считают что фиолетовый оттенок появлется только у нечистых кристаллов. Для получения хлорида вольфрама пользуются различными соединениями вольфрама, причем в качестве хлорирующих агентов можно применять не только газообразный хлор, но и различные соединения хлора : хлористый водород, фосген, пятихлористый фосфор, сера и.др. Водой хлористый вольфрам, так же как и хлорокись вольфрама, разлагается с образованием вольфрамовой кислоты. Легкость образования хлоридов и оксихлоридов вольфрама при сравнительно низких температурах используется в технологии при анализе вольфрама.
Получение
Существует несколько методов получения рассматриваемого соединения.
Первый — углеродное насыщение вольфрама. В результате на поверхности вольфрамовых частиц образуется монокарбид. Из него диффундирует углерод, формируя слой полукарбидного состава.
Для данных работ применяют вольфрамовый порошок и сажу. Данные материалы смешивают в определенном соотношении, наполняют ими, утрамбовывая, емкости и ставят в печь. Во избежание окисления операцию производят в водородной среде, так как в результате взаимодействия данного элемента с углеродом при 1300°С формируется ацетилен. Рассматриваемая технология предполагает формирование карбида вольфрама преимущественно за счет углерода. Температурный режим определяется гранулометрическим составом порошка. Так, для мелкозернистого используется температурный интервал 1300 — 1350°С, для крупнозернистого — 1600°С. Длительность выдержки равна 1 — 2 ч. В завершении получается карбид вольфрама, представленный немного спекшимися блоками.

Вольфрам
Второй вариант — углеродное восстановление вольфрамового оксида с карбидизацией. Данный метод предполагает совмещение карбидизации и восстановления. Процесс идет в среде CO и водорода.
Кроме того, карбид вольфрама получают из газовой фазы путем осаждения. Такое производство предполагает разложение при 1000°С карбонила вольфрама.
Восстановление вольфрамовых соединений с карбидизацией. Данную операцию осуществляют путем нагрева в водородной среде смеси паравольфрамата аммония либо вольфрамового ангидрида и вольфрамовой кислоты при 850 — 1000°С.
Наконец, выращивают кристаллы данного соединения из расплава. При этом используют смесь из Co и 40% монокарбида. Ее расплавляют при 1600°С в тигле из оксида алюминия. После гомогенизации температуру постепенно (1 — 3°С/мин) снижают до 1500°С и выдерживают 12 ч. Далее материал охлаждают и в кипящей соляной кислоте растворяют матрицу.
Кроме того, большие монокристаллы (до 1 см) выращивают по методу Чохральского.
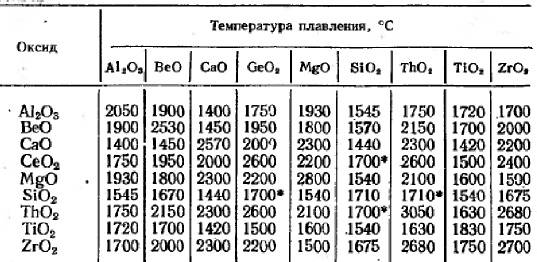
Основные металлические карбиды
На практике широко применяется множество карбидных соединений. Рассмотрим основные из них.
Карбид гафния
Встречается в виде только одного вещества — HfC. В нормальных условиях обладает кристаллической структурой, окрашено в серый цвет. плавится при температуре 3900 градусов — интересно, что его закипание происходит уже при температуре 4160 градусов. Поэтому к расплавлению нужно подходить аккуратно, чтобы не испарить его. При нагреве до 2000 градусов начинает взаимодействовать с металлами (молибден, вольфрам). Вещество не обладает полной химической инертностью — оно вступает в реакцию с кислотами (в азотной или серной кислоте оно способно полностью раствориться).
Карбиды хрома
Встречается в виде нескольких веществ; основные — Cr23C6, Cr3C2, Cr7C3. Отличаются высокой химической инертностью (хотя могут реагировать с цинком при сильном нагреве). Не вступают в контакт с водой, атмосферным воздухом, кислотами, щелочами, солями, другими карбидными соединениями. Температура плавления не слишком высокое — большинство соединений плавятся уже при температуре 1500-1700 градусов. У соединения Cr7C3 при нагреве до 800 градусов происходит ряд эндотермических реакций и превращений, что приводит к превращению вещества в Cr23C6.
Карбид титана
Встречается в виде одного стабильного соединения — TiC. При нормальных условиях обладает серым цветом с характерным металлическим блеском. Плавится при температуре 3100 градусов, кипит — при 4305 градусах. Обладает высокой устойчивостью, прочностью. Химическая инертность средняя — в нормальном состоянии может вступать в реакцию с кислотами и щелочами (хотя реакция идет слабо). При нагреве до 2500 градусов может вступать в реакцию с азотом (в том числе — атмосферным). При нагреве до 1200 градусов может окисляться и/или вступать в реакцию с углекислым газом.
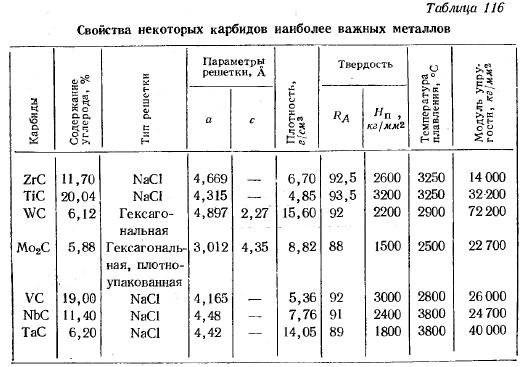
Карбиды вольфрама
Встречается в виде двух устойчивых соединений — WC и W2C. Оба карбида отличаются приблизительно одинаковыми химико-физическими свойствами. Вид — мелкий порошок серовато-черного цвета (со слабым металлическим блеском или без него). Вещества плавятся при температуре около 2720 градусов, однако при более низких температурах начинается их активных контакт с атмосферным воздухом, азотом или углекислым газом. Соединения легко растворяются в разогретых до температуре кипения серных и азотных кислотах.
Карбид кальция
Основное устойчивое соединение — CaC2. Вид — крупные прозрачные кристаллы, которые могут обладать светло-голубым оттенком. При наличии примесей может окрашиваться в другие цвета — серый, желтый, коричневый, черный и другие (в зависимости от типа примеси и ее концентрации). Соединение плавится при температуре порядка 2500 градусов, однако при комнатной температуре оно активно вступает в реакцию с водой с активным выделением ацетилена. Поэтому вещество нуждается в особых безопасных способах хранения (ацетилен является токсичным для человека).
Карбид циркония
Основное соединение — ZrC. Стандартное состояние — небольшие кристаллы серого цвета, обладающие металлическим блеском. Температура плавления — 3530 градусов, однако при нагреве до 1200 градусов вещество начинает активно вступать в реакцию с атмосферным кислородом, что приводит к образованию оксидов. Вещество слабо реагирует с кислотами, щелочами и солями, однако может вступать в реакцию с атомизированным азотом в составе сложных веществ, что приводит к образованию нитритов. Поэтому вещество нуждается в особых способах хранения.

Переработка вольфрамового сырья.
Первичная руда содержит около 0,5% оксида вольфрама. После флотации и отделения немагнитных компонентов остается порода, содержащая порядка 70% WO3. Затем обогащенная руда (и окисленный лом вольфрама) выщелачивается с помощью карбоната или гидроксида натрия:
4FeWO4 + O2 + 4Na2CO3 = 4NaWO4 + 2Fe2O3 + 4CO2
6MnWO4 + O2 + 6Na2CO3 = 6Na2WO4 + 2Mn3O4 + 6CO2
WO3 + Na2CO3 = Na2WO4 + CO2
WO3 + 2NaOH = Na2WO4 + H2O
Na2WO4 + CaCl2 = 2NaCl + CaWO4Ї.
Полученный раствор освобождается от механических примесей, а затем подвергается переработке. Первоначально осаждается вольфрамат кальция с последующим его разложением соляной кислотой и растворением образовавшегося WO3 в водном аммиаке. Иногда очистку первичного вольфрамата натрия осуществляют с помощью ионообменных смол. Конечный продукт процесса – паравольфрамат аммония:
CaWO4 + 2HCl = H2WO4Ї + CaCl2
H2WO4 = WO3 + H2O
WO3 + 2NH3·H2O(конц.) = (NH4)2WO4 + H2O
12(NH4)2WO4 + 14HCl(оч.разб.) = (NH4)10H2W12O42 + 14NH4Cl + 6H2O
Другим способом выделения вольфрама из обогащенной руды является обработка хлором или хлороводородом. Этот метод основан на относительно низкой температуре кипения хлоридов и оксохлоридов вольфрама (300° С). Способ применяется для получения особо чистого вольфрама.
Вольфрамитовый концентрат может быть сплавлен непосредственно с углем или коксом в камере с электрической дугой. При этом получают ферровольфрам, который используется при изготовлении сплавов в сталелитейной промышленности. Чистый концентрат шеелита также может быть добавлен в расплав стали.
Около 30% мирового потребления вольфрама обеспечивается за счет переработки вторичного сырья. Загрязненный лом карбида вольфрама, стружки, опилки и остатки порошкового вольфрама окисляются и переводятся в паравольфрамат аммония. Лом быстрорежущих сталей утилизируют в производстве этих же сталей (до 60–70% всего расплава). Лом вольфрама из ламп накаливания, электродов и химических реактивов практически не перерабатывается.
Основным промежуточным продуктом в производстве вольфрама является паравольфрамат аммония (NH4)10W12O41·5H2O. Он является и основным транспортируемым соединением вольфрама. Прокаливая паравольфрамат аммония, получают оксид вольфрама(VI), который затем обрабатывают водородом при 700–1000° С и получают порошок металлического вольфрама. Спеканием его с углеродным порошком при 900–2200° С (процесс цементации) получают карбид вольфрама.
В 2002 цена паравольфрамата аммония – основного коммерческого соединения вольфрама – составляла около 9000 долл. за тонну в пересчете на металл. В последнее время появилась тенденция к снижению цен на вольфрамовую продукцию вследствие большого предложения со стороны Китая и стран бывшего СССР.
В России вольфрамовые продукты производят: Скопинский гидрометаллургический завод «Металлург» (Рязанская область, вольфрамовый концентрат и ангидрид), Владикавказский Завод «Победит» (Северная Осетия, вольфрамовый порошок и слитки), Нальчикский Гидрометаллургический завод (Кабардино-Балкария, металлический вольфрам, карбид вольфрама), Кировградский завод твердых сплавов (Свердловская область, карбид вольфрама, вольфрамовый порошок), Электросталь (Московская область, паравольфрамат аммония, карбид вольфрама), Челябинский Электрометаллургический завод (ферровольфрам).
Карбиды вольфрама
Твердые сплавы рассмотрим более подробно. Тугоплавкий металл может образовывать разные карбиды: полукарбид и монокарбид. Они отличаются способностью растворять в себе тугоплавкие металлы и взаимодействием с разными кислотами.
Вольфрам — металл имеющий разные карбиды
Также монокарбид уступает поликарбиду в устойчивости и твердости. А к преимуществам монокарбида можно отнести способность к образованию кристаллов в расплавленном вольфраме, что дает возможность использовать его в минералокерамических изделиях. Полукарбид обладает большей устойчивостью к температурам, легкостью внедрения в твердые растворы монокарбида с другими металлами (феррумом, кобальтом), повышенной износоустойчивостью.
Это интересно: Как правильно закалить нож в домашних условиях
Область применения
Из-за своих уникальных свойств вольфрам получил широкое применение. В промышленности он применяется в чистом виде и в сплавах.
Основными областями применения являются:
Стали специальные. При производстве быстрорежущих сталей и для инструментальных сталей этот материал применяется в качестве легирующего элемента или же основного компонента. Из таких сталей производят штампы, пуансоны, фрезы, свёрла и прочие. Буква «Р» в названии сплава означает, что это быстрорежущая сталь, а буквы «К» или «М» — сталь легированная кобальтом или молибденом. Вольфрам ещё входит в состав сталей магнитных, которые подразделяются на вольфрам кобальтовые и вольфрамовые.
Сплавы твёрдые на основе карбида вольфрама. Это соединение углерода и вольфрама. Он тугоплавкий, износостойкий и имеет высокую твёрдость. Из него изготавливают рабочие части буровых и режущих инструментов.
Износостойкие и жаропрочные сплавы. В них использована тугоплавкость вольфрама. Наиболее распространёнными являются хромовые и кобальтовые соединения — стеллиты. Обычно их при помощи наплавки наносят на сильно изнашивающиеся машинные детали.
Тяжёлые и контактные соединения. К ним относят сплавы вольфрама с серебром и медью. Это довольно эффективные контактные материалы для производства рабочих частей выключателей, рубильников, электродов для точечной сварки и прочих оборудований.
Электроосветительная и электровакуумная техника. Вольфрам в виде разных кованых деталей, ленты или проволоки используют в производстве рентгенотехники, радиоэлектроники и электроламп. Это лучший материал для спиралей и нитей накаливания. Вольфрамовые прутки и проволоки служат для высокотемпературных печей электронагревателями. Эти электронагреватели могут работать в атмосфере инертного газа, водорода или вакуума.
Сварочные электроды
Сварка является важной сферой для применения этого металла. Из него делают электроды для сварки дуговой, так как они неплавкие.
https://youtube.com/watch?v=jmjsaMmSNwo
Биологическая роль
Вольфрам не играет значительной биологической роли. У некоторых архебактерий и бактерий имеются ферменты, включающие вольфрам в своем активном центре. Существуют облигатно-зависимые от вольфрама формы архебактерий-гипертермофилов, обитающие вокруг глубоководных гидротермальных источников. Присутствие вольфрама в составе ферментов может рассматриваться как физиологический реликт раннего архея — существуют предположения, что вольфрам играл роль в ранних этапах возникновения жизни.
Пыль вольфрама, как и большинство других видов металлической пыли, раздражает органы дыхания.