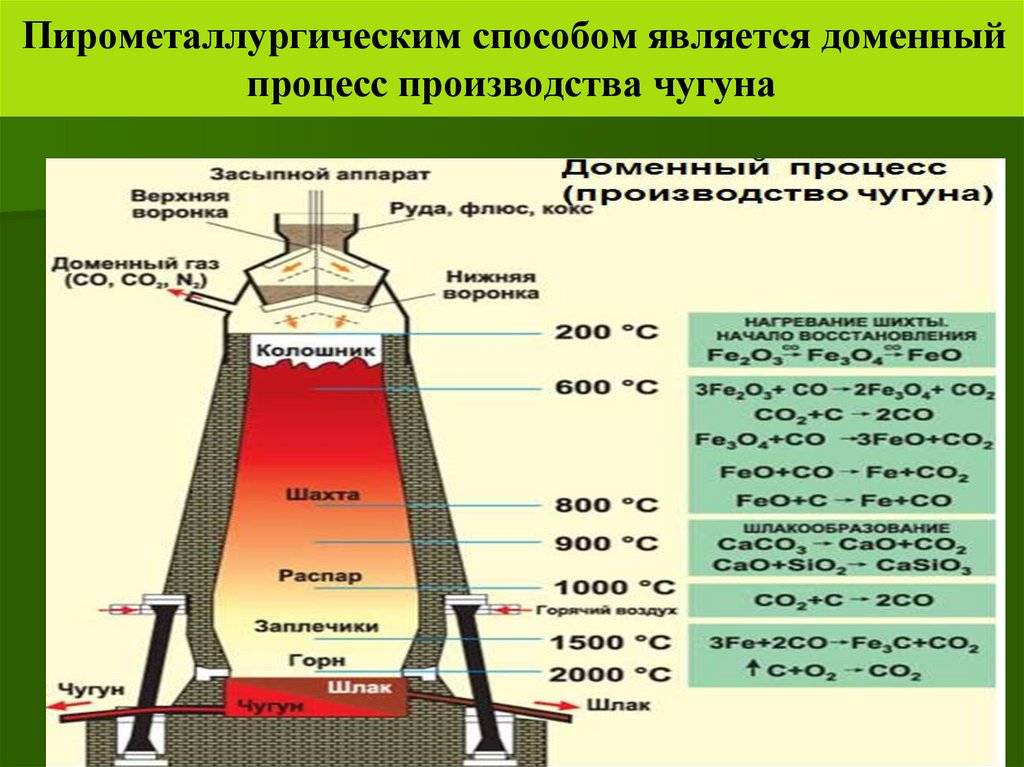
Природные соединения с содержанием меди
Чистая медь, которую собой представляют ее самородки, представлена в природе в очень незначительных количествах. В основном медь в природе присутствует в виде различных соединений, наиболее распространенными из которых являются следующие.
- Борнит – минерал, получивший свое название в честь ученого из Чехии И. Борна. Это сульфидная руда, химический состав которой характеризует ее формула – Cu5FeS4. Борнит имеет и другие названия: пестрый колчедан, медный пурпур. В природе эта руда представлена в двух полиморфных видах: низкотемпературной тетрагонально-скаленоэдрической (температура меньше 228 градусов) и высокотемпературной кубически-гексаоктаэдрической (больше 228 градусов). Данный минерал может иметь различные виды и в зависимости от своего происхождения. Так, экзогенный борнит – это вторичный ранний сульфид, который очень неустойчив и легко разрушается при выветривании. Второй тип – эндогенный борнит – характеризуется непостоянством химического состава, в котором могут присутствовать халькозин, галенит, сфалерит, пирит и халькопирит. Теоретически минералы данных видов могут включать в свой состав от 25,5% серы, более 11,2% железа и свыше 63,3% меди, но на практике такое содержание этих элементов никогда не выдерживается.
- Халькопирит – минерал, химический состав которого характеризуется формулой CuFeS2. Халькопирит, имеющий гидротермальное происхождение, раньше называли медным колчеданом. Наряду со сфалеритом и галенитом он входит в категорию полиметаллических руд. Данный минерал, который, кроме меди, содержит в своем составе железо и серу, формируется в результате протекания метаморфических процессов и может присутствовать в двух типах медных руд: контактово-метасоматического вида (скарны) и горные метасоматические (грейзены).
- Халькозин – сульфидная руда, химический состав которой характеризуется формулой Cu2S. Такая руда содержит в своем составе значительное количество меди (79,8%) и серу (20,2%). Эту руду часто называют «медным блеском», что объясняется тем, что ее поверхность выглядит как отблескивающий металл, обладающий различными оттенками – от свинцово-серого до совершенно черного. В медесодержащих рудах халькозин выглядит как плотные или мелкозернистые включения.

Халькопирит
В природе встречаются и более редкие минералы, которые содержат в своем составе медь.
- Куприт (Cu2O), относящийся к минералам оксидной группы, часто можно встретить в местах, где есть малахит и самородная медь.
- Ковеллин – сульфидная порода, сформированная метасоматическим путем. Впервые этот минерал, содержание меди в котором составляет 66,5%, был обнаружен в начале позапрошлого столетия в окрестностях Везувия. Сейчас ковеллин активно добывают на месторождениях в таких странах, как США, Сербия, Италия, Чили.
- Малахит – минерал, хорошо известный всем как поделочный камень. Наверняка все видели изделия из этого красивейшего минерала на фото или даже являются их обладателями. Малахит, который в России очень популярен, – это углекислая медная зелень или дигидрококскарбонат меди, относящийся к категории полиметаллических медесодержащих руд. Найденный малахит свидетельствует о том, что рядом есть месторождения других минералов, содержащих медь. В нашей стране крупное месторождение этого минерала находится в районе Нижнего Тагила, раньше его добывали и на Урале, но сейчас его запасы там значительно истощены и не разрабатываются.
- Азурит – минерал, который из-за своего синего цвета также называют «медной лазурью». Он характеризуется твердостью 3,5–4 единицы, основные его месторождения разрабатываются в Марокко, Намибии, Конго, Англии, Австралии, Франции и Греции. Азурит часто сращивается с малахитом и залегает в тех местах, где поблизости расположены месторождения медесодержащих руд сульфидного типа.

Малахит
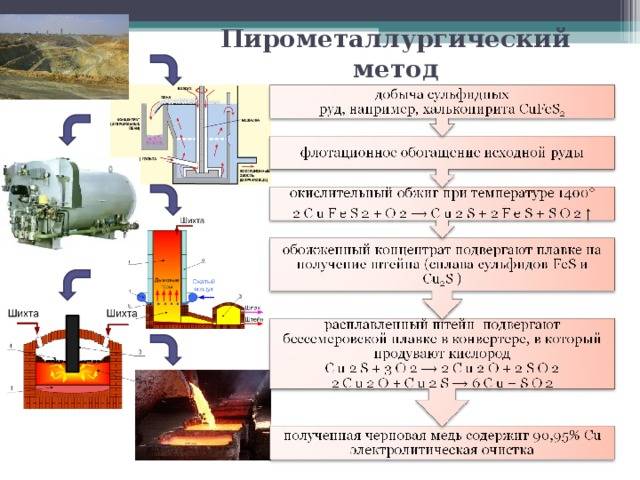
Что такое пирометаллургия?
Пирометаллургия – это отрасль науки и техники, связанная с использованием высоких температур для извлечения и очистки металлов. Следовательно, это отрасль добывающей металлургии. Этот процесс позволяет производить чистые металлы, подходящие для прямых продаж, и сплавы, подходящие в качестве сырья для дальнейшей обработки. Пирометаллургические процессы можно разделить на следующие категории в зависимости от техники: кальцинирование, обжиг, плавка и рафинирование.
Прокаливание или прокаливание – это термическое разложение материала. Этот процесс осуществляется в камерах, способных выдерживать большие затраты энергии. Например, печи, такие как шахтные печи, вращающиеся печи и реакторы с псевдоожиженным слоем.
Обжарка включает термические газо-твердые реакции. В этом процессе используются такие методы, как окисление, восстановление, хлорирование и сульфирование. Кроме того, этот метод в основном подходит для сульфидных руд металлов. Здесь сульфид металла нагревается в присутствии воздуха до высокой температуры; Эта температура может вызвать реакцию кислорода в воздухе с сульфидом с образованием диоксида серы, который покидает оксид металла.

Плавка – это термический процесс, при котором, наконец, один продукт находится в расплавленном состоянии. Затем оксиды металлов плавятся путем нагревания вместе с коксом (или древесным углем), что позволяет выделять диоксид углерода. Остается очищенный минерал. Рафинирование – это удаление примесей из руды с помощью термических процессов.
Плавку на штейн
Плавку на штейн ведут в отражательных или электрических печах при температуре 1250 – 1300 °С. В плавку поступают обожженные концентраты медных руд, в ходе нагревания которых протекают реакции восстановления оксида меди и высших оксидов железа
6CuO + FeS = 3Cu2O + FeO + SO2
FeS + 3Fe3O4 + 5SiO2 = 5(2FeO·SiO2) + SO2
В результате взаимодействия Cu2O с FeS образуется Cu2S по реакции:
Cu2O + FeS = Cu2S + FeO
Сульфиды меди и железа, сплавляясь между собой, образуют штейн, а расплавленные силикаты железа, растворяя другие оксиды, образуют шлак. Штейн содержит 15 – 55% Cu; 15 – 50% Fe; 20 – 30% S. Шлак состоит в основном из SiO2, FeO, CaO, Al2O3.
Штейн и шлак выпускают по мере их накопления через специальные отверстия.
Способы получения металлов
В зависимости от того, кокой восстановитель используют в металлургическом процессе различают: пиро – , гидро, электро – и биометаллургию.
Наиболее распространенные способы получения металлов: пирометаллургический и электрометаллургический. Большинство реакций восстановления протекают при высоких температурах (Рис. 2). Так как металлическая связь обладает повышенной прочностью, то выделение металлов в чистом виде из природных соединений проводят при высоких температурах.
Рис. 2. Металлургическое производство
Пирометаллургический способ
Пирометаллургия — получение металлов из руд при высоких температурах при участии восстановителей. В переводе с греческого «пирос» означает «огненный». Используют в качестве восстановителей кокс, диоксид углерода, водород. Применяют активные металлы для получения менее активных.
Пирометаллургия подразделяется на
- карботермия,
- водородотермия,
- металлотермию.
Карботермия: перевод сульфида металла путем обжига в оксид и дальнейшим восстановлением углем до чистого состояния.
2ZnS + 3O2 = 2ZnO + 2 SO2
ZnO + C = CO + Zn
Руды, состоящие из оксидов и сульфидов железа, подвергают карботермии. Проводят восстановление коксом или диоксидом углерода (угарным газом). Получают сплавы железа — чугун и сталь. Первый содержит больше углерода, а также оксидов серы, фосфора и кремния. Углерод снижает твердость и другие характерные для металлов качества.
Химические реакции, лежащие в основе выплавки чугуна:
- C + O2 = CO2↑,
- CO2 + C 2CO↑,
- 3Fe2O3 + CO = 2Fe3O4+ CO2↑,
- Fe3O4 + CO = 3FeO + CO2↑,
- FeO + CO = Fe + CO2↑.
Сталь выплавляют в специальных печах — электрических, конвертерных, мартеновских (Рис. 3). При продувании обогащенного кислородом воздуха выгорает избыточный углерод, его содержание уменьшается до 2% и ниже. Этот способ является более экономически применим, т.к. при помощи него получают сталь и чугун, которые широко используются в современной промышленности.
Рис. 3. Пирометаллургия
Восстановлением углем можно получить железо, медь, цинк, кадмий, германий, олово, свинец и другие металлы. В качестве сырья используют медную (Cu2O), оловянную (SnO2), марганцевую (MnO2) руды.
| Схема получение железа и хрома | (Cr2Fe)O4 + 4C(кокс) = Fe + 2Cr + 4CO↑ |
| Реакция, лежащая в основе выплавки меди | Cu2O + C (кокс) = 2Cu + CO↑ |
| Схема производство олова | SnO2 + 2C (кокс) = Sn + 2CO↑ |
| Процесс выплавки марганца | MnO2 + C(кокс) = Mn + CO2↑ |
| Схема получения свинца | 2PbO + C → Pb + CO↑ |
Металлы можно извлечь из сульфидных руд. Сначала проводят обжиг, затем — восстановление полученного оксида углем. Схемы обжига цинковой обманки и получение цинка:
- 2ZnS +3O2 = 2ZnO + 2SO2↑;
- ZnO + C = Zn + CO↑.
Карбонаты тоже прокаливают с углем для получения оксидов и последующего восстановления углем. Схемы обжига сидерита и восстановления оксида железа:
- FeCO3 = FeO + CO2↑;
- FeO + C = Fe + CO↑.
Водородотермия — производство металлов восстановлением водородом
Достоинством этого металлургического метода является получение очень чистых металлов. Восстановление меди из оксида CuO — пример восстановительных свойств водорода из школьного курса неорганической химии. Схема протекания реакции (Рис 4):
Рис. 4. Восстановление меди водородом
Водородом восстанавливают из оксидов тугоплавкие металлы молибден и вольфрам.
Металлотермия
Проводят восстановление одного металла другим, более химически активным. Этот способ применяют для получения металлов из оксидов и галогенидов.
В зависимости от природы металла-восстановителя различают алюминотермию, или алюмотермию, — восстановление алюминием и магнийтермию — восстановление магнием.
| Схема получение марганца | 3MnO2 + 4Al = 3Mn + 2Al2O3 |
| Процесс выплавки хрома | Cr2O3 + 2Al → 2Cr + Al2O3 |
| Схема получение кальция | 4CaO+ 2Al= 2Ca+ (CaAl2)O4 |
Силикотермия — восстановление металлов кремнием. Процесс протекает согласно схеме: 2MgO + Si → 2Mg + SiO2.
Виды сплавов
Несмотря на такое многообразие сплавов, наибольшее значение для людей играют те, основу которых составляет железо и алюминий. Именно они чаще всего встречаются в повседневной жизни. Виды сплавов бывают различными. Причем их разделяют по нескольким критериям. Так применяются различные способы изготовления сплавов. По данному критерию их делят на:
• Литые, которые получены путем кристаллизации расплава смешанных компонентов.
• Порошковые, созданные при помощи прессования смеси порошков и последующего спекания при высокой температуре. Причем зачастую компонентами таких сплавов являются не только простые химические элементы, но и их различные соединения, такие как карбиды титана или вольфрама в твердых сплавах. Их добавление в тех или иных количествах изменяет свойства металлических материалов.
Способы получения сплавов в виде готового изделия или заготовки разделяют на:
• литейные (силумин, чугун);
• деформируемые (стали);
• порошковые (титан, вольфрам).

Оборудование
Для получения и обработки применяется разное оборудование:
- Для термической обработки — печи, плавильни, горны.
- Для изменения шероховатостей поверхностей — шлифовальные станки, пескоструи.
- Для создания углублений, обработки кромок, торцов — долбежные, сверлильные, фрезеровальные станки.
- Для придания простой или сложной цилиндрической формы — токарные станки.
- Для разрезания заготовок — пилы, лазерные или гидроабразивные резаки.
Современное оборудование оснащается автоматическими системами управления, что ускоряет производство, минимизирует физические затраты со стороны человека.
Самодельный горн (Фото: Instagram / vetal7070)
Особенности медных руд
Медьсодержащие руды характеризуются как многоэлементные. Наиболее часто встречающиеся соединения бывают с:
- железом;
- серой;
- медью.
В незначительной концентрации могут присутствовать:
- никель;
- золото;
- платина;
- серебро.
Месторождения во всем мире имеют примерно одинаковый набор химических элементов в составе руды, отличаются лишь их процентным соотношением. Чтобы получить чистый металл, используют различные промышленные способы. Почти 90% металлургических предприятий используют одинаковый метод производства чистой меди – пирометаллургический.

Один из самых больших карьеров по добыче руди приносит 17 миллионов тонн меди в год
Схема этого процесса позволяет также получать металл из вторичного сырья, что для промышленности является существенным плюсом. Поскольку месторождения относятся к группе не восполняемых – запасы с каждым годом уменьшаются, руды беднеют, а их добыча и производство становится дорогим. Это, в конечном счете, влияет на цену металла на международном рынке. Кроме пирометаллургического метода, существуют еще способы:
- гидрометаллургический;
- метод огневого рафинирования.
Стадии пирометаллургического производства меди
Общие способы получения метала из руды
Промышленное получение меди с использованием пирометаллургического способа имеет преимущества перед другими методами:
- технология обеспечивает высокую производительность – с ее помощью можно получать метал из породы, в которой содержание меди даже ниже 0,5%;
- позволяет эффективно перерабатывать вторичное сырье;
- достигнута высокая степень механизации и автоматизации всех этапов;
- при его использовании значительно сокращаются выбросы вредных веществ в атмосферу;
- метод экономичный и эффективный.
Обогащение
Схема обогащения руды
На первом этапе производства необходимо подготовить руду, которую доставляют на обогатительные комбинаты прямо с карьера или шахты. Часто встречаются большие куски породы, которые предварительно нужно измельчить.
Происходит это в огромных дробильных агрегатах. После дробления получается однородная масса, с фракцией до 150 мм. Технология предварительного обогащения:
- в большую емкость засыпается сырье и заливается водой;
- затем добавляется кислород под давлением, чтобы образовалась пена;
- частицы металла прилипают к пузырькам и поднимаются наверх, а пустая порода оседает на дне;
- далее, медный концентрат отправляется на обжиг.
Обжиг
Этот этап направлен на то, чтобы максимально снизить содержание серы. Рудную массу помещают в печь, где устанавливается температура 700–800оС. В результате термического воздействия содержание серы сокращается в два раза. Сера окисляется и испаряется, а часть примесей (железа и других металлов) переходит в легкошлакуемое состояние, которое облегчит в дальнейшем плавку.
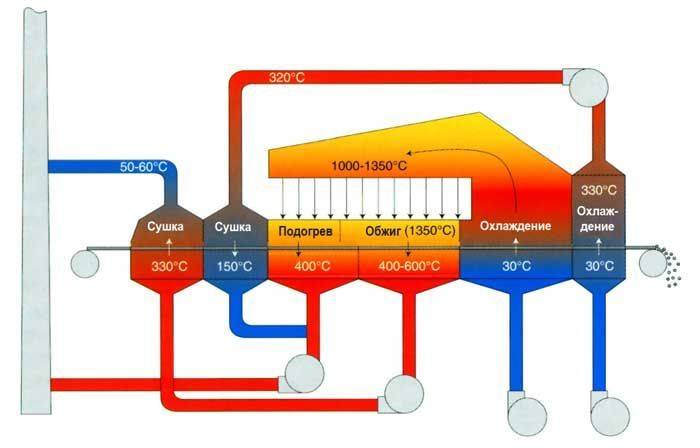
Обжиг руды для снижения уровня серы
Плавка на штейн
Технология плавки на штейн позволяет получить черновую медь, которая различается по маркам: от МЧ1 – самая чистая до МЧ6 (содержит до 96% чистого металла). В ходе процесса плавки, сырье погружается в специальную печь, в которой температура поднимается до 1450оС.

Технология переработки медной руды и получение черной меди
После расплавления массы она продувается сжатым кислородом в конвертерах. Они имеют горизонтальный вид, а дутье осуществляется через боковое отверстие. В результате продува сульфиды железа и серы окисляются и переводятся в шлак. Тепло в конвертере образуется за счет протекания раскаленной массы, он дополнительно не нагревается. Температура при этом составляет 1300оС.
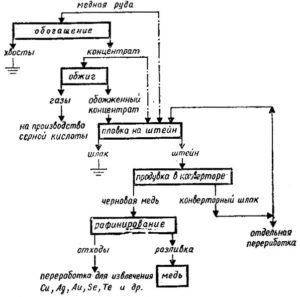
Общая схема выплавки меди
На выходе из конвертера получают черновой состав, который содержит до 0,04% железа и 0,1% серы, а также до 0,5% прочих металлов:
- олова;
- сурьмы;
- золота;
- никеля;
- серебра.
Такой черновой металл отливается в слитки массой до 1200 кг. Это так называемая анодная медь. Многие производители останавливаются на этом этапе, реализуют такие слитки. Но поскольку часто производство меди сопровождается добычей драгоценных металлов, которые содержатся в руде, то на обогатительных комбинатах используется технология рафинирования чернового сплава. При этом выделяются и сохраняются прочие металлы.
Рафинирование с использованием катодной меди
Технология получения рафинированной меди довольно простая. Ее принцип используют даже для чистки медных монет от окислов в домашних условиях. Схема производства выглядит следующим образом:

Слитки рафинированной меди
- черновой слиток помещается в ванну с электролитом;
- в качестве электролита используется раствор со следующим содержанием:
- сульфат меди – до 200 г/л;
- серная кислота – 135–200 г/л;
- коллоидные добавки (тиомочевина, столярный клей)– до 60 г/л;
- вода.
- температура электролита должна быть до 55оС;
- помещаются в ванну пластины катодной меди – тонкие листы чистого металла;
- подключается электричество. В это время происходит электрохимическое растворение металла. Частицы меди концентрируются на катодной пластине, а прочие включения оседают на дне и называются шлам.
Весь процесс электролиза протекает в течение 20–28 суток. За этот период вынимают катодную медь до 3–4 раз. Вес пластин получается до 150 кг.
Как это делается: добыча меди
В процессе рафинирования, на катодной меди могут образовываться дендриты – наросты, которые сокращают расстояние до анода. В результате чего снижается скорость и эффективность реакции. Поэтому, при возникновении дендритов, их незамедлительно удаляют.
Что такое гидрометаллургия?
Гидрометаллургия – это отрасль промышленной химии, в которой мы используем водный раствор для извлечения металла из руды, концентратов, переработанного или остаточного материала и т. Д. В гидрометаллургии есть три основных области: выщелачивание, концентрирование и очистка, а также извлечение металла.
Процесс выщелачивания можно проводить разными способами, например: на месте выщелачивание, кучное выщелачивание, чановое выщелачивание, выщелачивание в резервуаре и выщелачивание в автоклаве. Это пять основных типов выщелачивания. В процессе выщелачивания используется водный раствор для извлечения металла из руды. Раствор, который используется специально в гидрометаллургии, называется выщелачивающим раствором. Он может иметь разные значения pH, окислительно-восстановительный потенциал, состав хелатирующего агента, температуру и другие свойства в зависимости от типа металла, который мы собираемся извлечь. Эти условия реакции меняются в зависимости от необходимости оптимизации скорости реакции, степени и селективности растворения и т. Д.
Следующий этап гидрометаллургии – это концентрирование и очистка раствора. Эта стадия включает концентрацию иона металла в выщелачиваемой жидкости и удаление нежелательных ионов металлов. Основными этапами, включенными в этот этап, являются осаждение, цементация, экстракция растворителем, ионный обмен и электрохимическое извлечение.
Стадия извлечения металла – заключительный этап гидрометаллургии. Металл, полученный на этом этапе, подходит для прямой продажи. Однако, когда нам нужен металл сверхвысокой чистоты, необходима дополнительная очистка. Извлечение металла может осуществляться двумя способами: электролизом и осаждением.
Применение железа
Примечательным можно считать тот факт, что из самого Феррума, в его химически чистой форме, в мире практически ничего не делается и не производится. Данный элемент очень легко окисляется, вступая в реакции в кислородом или другими элементами. Так для чего нужна железная руда? Все просто. Феррум, обогащенный карбоном (сплав чугуна) – весьма и весьма популярный материал. Чугун может или служить самостоятельной единицей для изготовления каких-либо вещей и предметов, или же быть промежуточным звеном между железом, и сталью.

Сталь – это сплав железа, углерода и других элементов. Железа должно быть не менее 45%, карбона – от 0,02 до 2,14 процента. Если выше 2,14% – это уже чугун. И уж сталь-то, в десятках своих вариаций, в наше время используется практически везде. Машиностроение, авиация, приборостроение, космические постройки, ядерная энергетика, медицина (существует даже термин – хирургическая сталь), оружейная отрасль (как холодное, так и огнестрельное), сельхозинвентарь, строительная продукция и т.д. За счет такой популярности стали, смело можно утверждать, что ни один металл периодической таблицы не используется так интенсивно и в таких количествах на Земле, как железо.
Действительно, сфер производства продукции железной руды, а также соединений и сплавов на основе Феррума – просто не счесть. Однако, в будущем, при таких темпах и масштабах добычи, перед человечеством могут встать два вопроса: что делать, когда запасы этого металла в недрах нашей планеты станут иссякать? И как поступать с теми гигантскими котлованами по всей планете, которые остаются после проведения добычи железной руды открытым способом?..
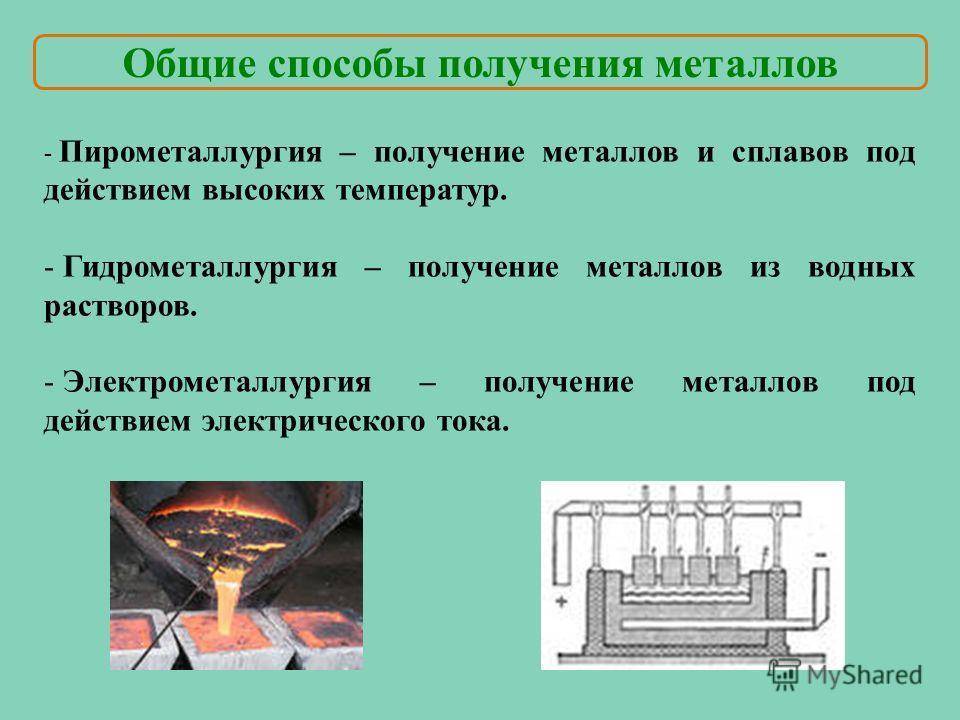
Общие способы получения металлов

Значительная химическая активность металлов (взаимодействие с кислородом воздуха, другими неметаллами, водой, растворами солей, кислотами) приводит к тому, что в земной коре они встречаются главным образом в виде соединений: оксидов, сульфидов, сульфатов, хлоридов, карбонатов и т. д. В свободном виде встречаются металлы, расположенные в ряду напряжений правее водорода (Аg, Нg, Рt,Аu, Сu), хотя гораздо чаще медь и ртуть в природе можно встретить в виде соединений.
Минералы и черные породы, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно, называют рудами.
Получение металлов из руд — задача металлургии.
Металлургия — это и наука о промышленных способах получения металлов из руд, и отрасль промышленности.
Любой металлургический процесс — это процесс восстановления ионов металла с помощью различных восстановителей. Суть его можно выразить так:
М n+ + ne−→M
Чтобы реализовать этот процесс, надо учесть активность металла, подобрать восстановитель, рассмотреть технологическую целесообразность, экономические и экологические факторы.
В соответствии с этим существуют следующие способы получения металлов:
• пирометаллургический;
• гидрометаллургический;
• электрометаллургический.
Пирометаллургия
Пирометаллургия — восстановление металлов из руд при высоких температурах с помощью углерода, оксида углерода (II), водорода, металлов — алюминия, магния.
Например, олово восстанавливают из касситерита SnО2, а медь — из куприта Cu2O
прокаливанием с углем (коксом):
Сульфидные руды предварительно подвергают обжигу при доступе воздуха, а затем полученный оксид восстанавливают углем:
Из карбонатных руд металлы выделяют также путем прокаливания с углем, т. к. карбонаты при нагревании разлагаются, превращаясь в оксиды, а последние восстанавливаются углем:
Восстановлением углем можно получить Fе, Сu, Zn, Сd, Ge, Sn, Рb и другие металлы, не образующие прочных карбидов (соединений с углеродом).
В качестве восстановителя можно применять водород или активные металлы:
1) МоO3 + ЗН2 = Мо + ЗН2O (водородотермия)
К достоинствам этого метода относится получение очень чистого металла.
2) TiO2+ 2Мg = Тi + 2МgO (магнийтермия)
ЗМnO2 + 4Аl = ЗМn + 2Аl2O3 (алюминотермия)
Чаще всего в металлотермии используют алюминий, теплота образования оксида
https://youtube.com/watch?v=_-nVROAFWAY
которого очень велика (2А1 + 1,5 O2 = Аl2O3 + 1676 кДж/моль). Электрохимический ряд напряжений металлов нельзя использовать для определения возможности протекания реакций восстановления металлов из их оксидов. Приближенно установить возможность этого процесса можно на основании расчета теплового эффекта реакции (Q), зная значения теплот образования оксидов:
Q= Σ Q1 — Σ Q 2 ,
где Q1— теплота образования продукта, Q2 -теплота образования исходного вещества.
Доменный процесс (производство чугуна):C + O2 = CO2, CO2 + C 2CO3Fe2O3 + CO = 2(Fe2Fe32)O4+ CO2(Fe2Fe32)O4+ CO= 3FeO + CO2FeO + CO= Fe + CO2(чугун содержит до 6,67% углерода в виде зерен графита и цементита Fe3C);
Выплавка стали (0,2-2,06% углерода) проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева.
Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов.
При этом оксиды либо улавливаются в виде отходящих газов (CO2, SO2), либо связываются в легко отделяемый шлак – смесь Ca3(PO4)2 и CaSiO3. Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Гидрометаллургия
Гидрометаллургия — это восстановление металлов из их солей в растворе.
Процесс проходит в два этапа: 1) природное соединение растворяют в подходящем реагенте для получения раствора соли этого металла; 2) из полученного раствора данный металл вытесняют более активным или восстанавливают электролизом. Например, чтобы получить медь из руды, содержащей оксид меди СuО, ее обрабатывают разбавленной серной кислотой:
СuО + Н2SО4 = СuSO4 + Н2
Затем медь либо извлекают из раствора соли электролизом, либо вытесняют из сульфата железом:
СuSO4. + Fе = Сu + FеSO4
Таким образом, получают серебро, цинк, молибден, золото, уран.
Электрометаллургия
Электрометаллургия — восстановление металлов в процессе электролиза растворов или расплавов их соединений.
Этим методом получают алюминий, щелочные металлы, щелочноземельные металлы. При этом подвергают электролизу расплавы оксидов, гидроксидов или хлоридов.
Примеры:а) NaCl (электролиз расплава) → 2Na + Cl2
Способы получения и добычи
Добыча и обработка проводится на природных рудниках. Потом расходное сырье доставляется до литейного предприятия, где происходит его переработка в конечный материал. Способы получения:
- Порошковый. При изготовлении сплавов используются порошки — смесь основных компонентов сплава по ГОСТу. С помощью специального оборудования порошок спрессовывается, ему придают определенную форму. После этого расходный материал спекают в промышленной печи.
- Литейный способ. Все компоненты будущего сплава сначала расплавляются, а потом перемешиваются. Смесь должна застыть.
Природные источники
Самое большое количество металлов содержится в земной коре. Их соединения можно найти в разных продуктах питания, воде, воздухе, химических веществах.
Природные соединения
Природные соединения:
- сульфиды — киноварь, цинковая обманка, серный колчедан;
- хлориды — каменная соль, сильвинит;
- сульфаты — гипс, глауберова соль;
- карбонаты — магнезит, доломит, известняк, мрамор, мел;
- оксиды — красный, магнитный, бурый железняк;
- нитраты — чилийская селитра.
Добыча руды (Фото: Instagram / dikomnw)
Способы добычи
Существует два способа добычи металлических руд:
- Открытый. Подразумевает разработку огромного карьера, который углубляется к центру. С его глубины на карьерных самосвалах руда вывозится наверх, где проходит дальнейшую переработку. Средняя глубина карьеров — 300 метров. Для разработки применяются крупные экскаваторы, земснаряды, карьерная техника. Карьерный метод добычи металлической руды применяется только, если после проверки почвы в ней было обнаружено более 57% руды. Главный недостаток карьера — малая глубина разработки.
- Закрытый. Подразумевает разработку шахт, которые могут уходить вниз на глубину нескольких сотен метров. Применяется, когда на поверхности после проверки было обнаружено менее 57% полезных руд. Внешне шахта напоминает колодец, который разветвляется в стороны на большой глубине. Главный недостаток — опасность для рабочих (частые обвалы, взрывы газов, большая вредность для здоровья).
Один из современных способов добычи металлической руды — СГД. Представляет собой гидромеханических метод добычи руды, который подразумевает создание глубокой шахты, снабженной трубопроводом с гидромонитором. Струя воды под большим напором подается в трубопровод. С ее помощью откалываются горные породы, которые всплывают наверх шахты. Эффективность данного способа небольшая, но он полностью безопасен для людей.
Шахта (Фото: Instagram / subcities)
Богатые рудники
Богатые железные рудники:
- Бакчарское железорудное месторождение.
- Абаканское железорудное месторождение.
- Абагасское железорудное месторождение.
- Курская магнитная аномалия.
Самые богатые месторождения алюминиевых руд находятся в
- Венгрии;
- Франции;
- Индии;
- Южной Африке;
- Казахстане;
- России;
- Югославии;
- Кольском полуострове;
- Сибири.
Богатые месторождения медной руды расположены в США, Швеции, Канаде, России, Финляндии, ЮАР.
Медная руда (Фото: Instagram / alex_tango1910)
Гидрометаллургия
Методика, которая основана на проведении химических реакциях. Они протекают в различных растворах. Наиболее распространенные материалы, которые получаются подобным способом — никель, цинк, золото.
Пирометаллургия
Из расходного сырья металл извлекается под воздействием высоких температур. Для проведения данного способа применяются печи, плавильни. Этим методом получают чугун, свинец, сталь, никель, медь, хром
Для изготовления активных металлов важно использовать восстановители
Электрометаллургия
Подразумевает обработку расходного сырья электрическим током. Сила тока изменяется зависимо от преобладающих в составе руды компонентов. С помощью электрометаллургии получаются разные металлы — щелочноземельные, щелочные. Основные из них — алюминий, магний.
- С помощью металлов. Этот процесс называют металлотермией.
- С помощью водорода. С помощью этой методики можно получить материал с наименьшим количеством посторонних вкраплений.
- С помощью углерода или оксида углерода. Эта методика называется карботермией.